





 Рейтинг: 4.3/5.0 (1842 проголосовавших)
Рейтинг: 4.3/5.0 (1842 проголосовавших)Категория: Бланки/Образцы

ПРИКАЗ Минздрава РФ от 25.12.97 N 380 "О СОСТОЯНИИ И МЕРАХ ПО СОВЕРШЕНСТВОВАНИЮ ЛАБОРАТОРНОГО ОБЕСПЕЧЕНИЯ ДИАГНОСТИКИ И ЛЕЧЕНИЯ ПАЦИЕНТОВ В УЧРЕЖДЕНИЯХ ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ"
ПОЛОЖЕНИЕ О КЛИНИКО-ДИАГНОСТИЧЕСКОЙ ЛАБОРАТОРИИ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКОГО УЧРЕЖДЕНИЯ И ЦЕНТРАЛИЗОВАННОЙ КЛИНИКО-ДИАГНОСТИЧЕСКОЙ ЛАБОРАТОРИИ
1. Клинико-диагностическая лаборатория (в дальнейшем - КДЛ) является диагностическим подразделением лечебно-профилактического учреждения (ЛПУ) и создается на правах отделения.
2. Централизованные КДЛ создаются по указанию соответствующих территориальных органов управления здравоохранением для выполнения как различных видов исследований, так и одного их вида: биохимические, иммунологические, цитологические, микробиологические и другие исследования (специализированные лаборатории).
3. Организационная структура и порядок финансирования централизованных КДЛ устанавливается органом управления здравоохранением с учетом выполняемых ими задач и в соответствии с договором об участии лабораторий в осуществлении территориальных медицинских программ.
4. КДЛ, независимо от подчиненности и формы собственности, должна иметь сертификат на избранный вид деятельности.
5. Руководство КДЛ осуществляет заведующий, назначаемый и освобождаемый от должности руководителем учреждения здравоохранения в установленном порядке.
6. Деятельность КДЛ регламентируется соответствующими нормативными документами и настоящим положением.
7. Штаты КДЛ устанавливаются в соответствии с действующими нормативными документами с учетом местных условий или рассчитываются в соответствии с объемом работы.
8. Оснащение КДЛ осуществляется в соответствии с профилем и уровнем лечебно-профилактического учреждения.
9. КДЛ размещается в специально оборудованных помещениях, полностью соответствующих требованиям правил по устройству, эксплуатации и техники безопасности.
10. Нагрузка персонала определяется задачами лаборатории, положением о его функциональных обязанностях, а также расчетными нормами времени на проведение лабораторных исследований.
11. Основными задачами КДЛ являются:
- проведение клинических лабораторных исследований в соответствии с профилем ЛПУ (общеклинических, гематологических, иммунологических, цитологических, биохимических, микробиологических и других, имеющих высокую аналитическую и диагностическую надежность) в объеме согласно заявленной номенклатуре исследований при аккредитации КДЛ в соответствии с лицензией ЛПУ. Объем выполняемых исследований не должен быть ниже минимального объема, рекомендуемого для ЛПУ данной мощности;
- внедрение прогрессивных форм работы, новых методов исследований, имеющих высокую аналитическую точность и диагностическую надежность;
- повышение качества лабораторных исследований путем систематического проведения внутрилабораторного контроля качества лабораторных исследований и участия в программе Федеральной системы внешней оценки качества (в дальнейшем - ФСВОК);
- оказание консультативной помощи врачам лечебных отделений в выборе наиболее диагностически информативных лабораторных тестов и трактовке данных лабораторного обследования больных;
- обеспечение клинического персонала, занимающегося сбором биологического материала, детальными инструкциями о правилах взятия, хранения и транспортировки биоматериала, обеспечивающими стабильность образцов и надежность результатов. Ответственность за точное соблюдение этих правил клиническим персоналом несут руководители клинических подразделений;
- повышение квалификации персонала лаборатории;
- проведение мероприятий по охране труда персонала, соблюдение техники безопасности, производственной санитарии, противоэпидемиологического режима в КДЛ;
- ведение учетно-отчетной документации в соответствии с утвержденными формами.
12. В соответствии с указанными задачами КДЛ осуществляет:
- освоение и внедрение в практику методов клинической лабораторной диагностики, соответствующих профилю и уровню лечебно-профилактического учреждения;
- проведение клинических лабораторных исследований и выдачу по их результатам заключений.
13. КДЛ имеет право:
- проводить на договорной основе лабораторные исследования для других ЛПУ;
- участвовать в других системах внешней оценки качества клинических лабораторных исследований;
- принимать участие в научных разработках, проводимых с использованием полученных в лаборатории данных (результаты исследований, полученные в лаборатории, являются ее интеллектуальной собственностью и не могут быть использованы без ее согласия).
Начальник Управления
организации медицинской
помощи населению
А.И.ВЯЛКОВ
УТВЕРЖДЕНО
приказ Минздрава РФ
от 25.12.97 N 380
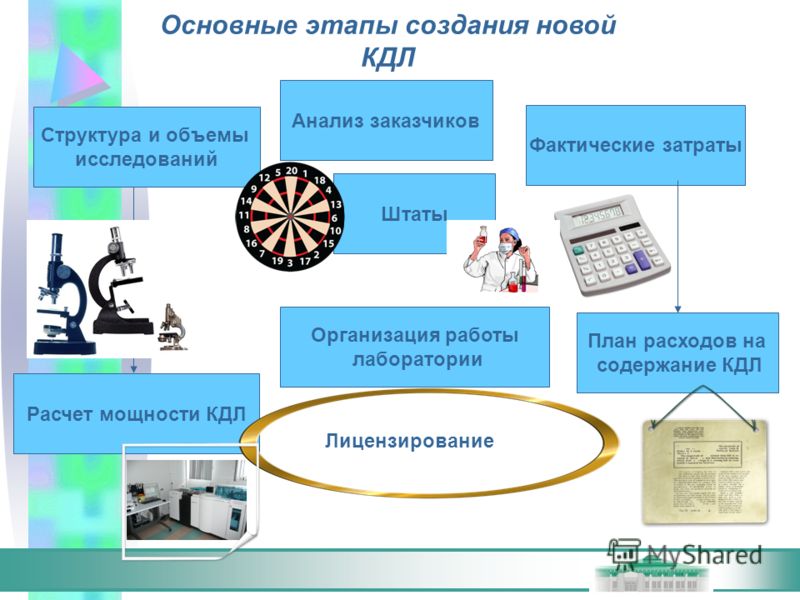
Современные представления о структуре лабораторной службы.
Организация работы в КДЛ. Материально-техническое оснащение КДЛ.
Спектр лабораторных исследований, выполняемых КДЛ. Ведение документации в КДЛ.
Порядок работы иммунологической лаборатории. Материально-техническое оснащение, спектр лабораторных исследований иммунологической лаборатории.
Порядок работы серологической лаборатории. Материально-техническое оснащение, спектр лабораторных исследований.
Цели и задачи иммунологической лаборатории, методики выполнения анализов в иммунологической лаборатории, ведение документации.
Цели и задачи серологической лаборатории, методики выполнения анализов, ведение документации.
Порядок работы ПЦР-лаборатории. Материально-техническое оснащение. Спектр лабораторных исследований.
Ведение документации в ПЦР-лаборатории, методики выполнения анализов, выполнение требований биологической безопасности.
Методики выполнения анализов в биохимической лаборатории, ведение документации.
1.1.Современные представления о структуре лабораторной службы
Служба клинической лабораторной диагностики является совокупностью клинико-диагностических лабораторий - подразделений учреждений здравоохранения, организованных и действующих в соответствии с едиными научно-методическими принципами.
В зависимости от структуры, профиля и мощности организаций здравоохранения
в их составе функционируют КДЛ:
КДЛ общего типа предназначены для выполнения рутинных (ординарных) лабораторных исследований – гематологических, биохимических, общеклинических и некоторых других с целью постановки диагноза заболевания, оценки тяжести его течения, прогноза и эффективности проводимой терапии.
Централизованные КДЛ преследуют решение таких задач, как проведение наиболее сложных и трудоемких лабораторных исследований; освоение и внедрение новых методов; проведение мероприятий по повышению качества лабораторных исследований; наиболее рациональное (экономное и эффективное) использование лабораторной техники, дорогостоящих реактивов и кадров специалистов.
Специализированные КДЛ. как правило, входят в состав специализированных учреждений: эндокринологических, кардиологических, онкологических, аллергологических и других.
1.2. Организация работы в КДЛ. Материально-техническое оснащение КДЛ
Министерство здравоохранения РФ
Положение о клинико-диагностической лаборатории лечебно-профилактического учреждения и централизованной клинико-диагностической лаборатории
1. Клинико-диагностическая лаборатория (в дальнейшем - КДЛ) является диагностическим подразделением лечебно-профилактического учреждения (ЛПУ) и создается на правах отделения.
2. Централизованные КДЛ создаются по указанию соответствующих территориальных органов управления здравоохранением для выполнения как различных видов исследований, так и одного их вида: биохимические, иммунологические, цитологические, микробиологические и другие исследования (специализированные лаборатории).
3. Организационная структура и порядок финансирования централизованных КДЛ устанавливается органом управления здравоохранением с учетом выполняемых ими задач и в соответствии с договором об участии лабораторий в осуществлении территориальных медицинских программ.
4. КДЛ. независимо от подчиненности и формы собственности, должна иметь сертификат на избранный вид деятельности.
5. Руководство КДЛ осуществляет заведующий, назначаемый и освобождаемый от должности руководителем учреждения здравоохранения в установленном порядке.
6. Деятельность КДЛ регламентируется соответствующими нормативными документами и настоящим положением.
7. Штаты КДЛ устанавливаются в соответствии с действующими нормативными документами с учетом местных условий или рассчитываются в соответствии с объемом работы.
8. Оснащение КДЛ осуществляется в соответствии с профилем и уровнем лечебно-профилактического учреждения.
9. КДЛ размещается в специально оборудованных помещениях, полностью соответствующих требованиям правил по устройству, эксплуатации и техники безопасности.
10. Нагрузка персонала определяется задачами лаборатории, положением о его функциональных обязанностях, а также расчетными нормами времени на проведение лабораторных исследований.
КДЛ, независимо от подчиненности и формы собственности, должна иметь сертификат на избранный вид деятельности
Штаты КДЛ устанавливаются в соответствии с действующими нормативными документами с учетом местных условий или рассчитываются в соответствии с объемом работы (приложение 12 к Приказу МЗ РФ №380 )
Оснащение КДЛ осуществляется в соответствии с профилем и уровнем лечебно-профилактического учреждения (приложение 8 к Приказу МЗ РФ №380 )
1.3. Спектр лабораторных исследований, выполняемых КДЛ. Ведение документации в КДЛ
Перечень документов, наличие которых обязательно для выполнения работ в КДЛ
1. Паспорт клинико-диагностической лаборатории, состоящий из титульного листа и следующих форм (таблиц):
1. Перечень выполняемых в КДЛ исследований.
2. Сведения об имеющихся средствах измерения (аппаратуре).
3. Сведения об имеющемся вспомогательном оборудовании.
4. Сведения об имеющихся стандартных контрольных материалах.
5. Сведения о мерной посуде, применяемой в клинико-диагностической лаборатории.
6. Сведения о штатном обеспечении и кадровом составе КДЛ.
7. Сведения о помещениях клинико-диагностической лаборатории.
Таблицы паспорта составляются по формам, предложенным при подготовке документации к аккредитации лабораторий, с некоторыми дополнениями:
В таблице 1 «Перечень выполняемых в КДЛ исследований» в графе 2 указывается вместе с наименованием исследования применяемый метод.
Таблица 6 («Сведения о штатном обеспечении и кадровом составе клинико-диагностической лаборатории») дополняется таблицей о штатном обеспечении, включающей графы:
– количество штатных должностей;
– количество занятых должностей;
– количество физических лиц, в том числе имеющих вторую, первую и высшую категорию,
– количество фельдшеров-лаборантов (лаборантов).
Паспорт КДЛ утверждается главным врачом ЛПУ.
2. Положение о клинико-диагностической лаборатории (должно быть утверждено приказом главного врача ЛПУ).
3. Должностные инструкции (функциональные обязанности) для каждой категории работников, на каждого сотрудника, утвержденные в установленном порядке.
4. Инструкции по санитарно-противоэпидемическому режиму для каждого участка, вида работ.
5. Инструкции по охране труда и технике безопасности для каждого участка, вида работ.
6. Инструкции по противопожарной безопасности.
Инструкции должны включать раздел о действиях персонала при различных видах аварий, должны быть утверждены главным врачом и председателем профкома ЛПУ, обновляться ежегодно и по необходимости.
Все сотрудники КДЛ должны быть ознакомлены с действующими инструкциями, делается отметка и подпись на должностных инструкциях и в журнале инструктажа по технике безопасности и санитарно-противоэпидемическому режиму. Рабочие экземпляры инструкции должны иметься на рабочих местах.
7. Нормативно-техническая документация, инструкции по эксплуатации средств измерений: приказы МЗ СССР об унификации методов исследований, инструкции к наборам реагентов, «Перечень методик выполнения измерений, применяемых в КДЛ ЛПУ», утвержденным Министерством здравоохранения (Приказ Минздрава РФ от 25.12.97 N 380 «О состоянии и мерах по совершенствованию лабораторного обеспечения диагностики и лечения пациентов в учреждениях здравоохранения Российской Федерации").
8. Описание используемых методов лабораторного анализа.
Если планируемый к использованию в лаборатории метод исследования не утвержден Перечнем и дополнением к нему, необходимо иметь в КДЛ копию Регистрационного удостоверения МЗ РФ о разрешении применения диагностического метода, диагностического набора, аппарата в медицинской практике на территории РФ.
Если исследование проводится в соответствии с методическими разработками, не утвержденными МЗ РФ (МЗ СССР), а опубликованными в научной литературе, справочниках и т.д. если используется существенная модификация утвержденной методики, – инструкция по выполнению такого исследования должна согласовываться с главным специалистом по клинической лабораторной диагностике региона и утверждаться главным врачом ЛПУ.
Папка с основными экземплярами методик хранится у заведующего клинико-диагностической лабораторией. Рабочие экземпляры должны быть на рабочих местах. Папки инструкций по проведению исследований должны включать протоколы построения калибровочных графиков. Калибровки проверяются каждое полугодие и по мере необходимости.
Результаты исследований выдаются клинико-диагностической лабораторией на бланках утвержденных образцов, с обязательным указанием единиц измерений, значений диапазона референтных (нормальных) величин, при необходимости - методик определения. Бланк результатов исследования датируется и подписывается исполнителем, ответственным сотрудником или заведующим клинико-диагностической лабораторией.
10. Журнал учета спирта.
11. Журнал учета сильнодействующих и ядовитых веществ.
12. Журнал учета проведения внутрилабораторного контроля качества.
В клинико-диагностической лаборатории должен проводиться ежедневный внутрилабораторный контроль качества (ВЛК) исследований по максимальному количеству анализов.
Необходимо оптимально использовать для ВЛК аттестованные контрольные материалы и помесячно оценивать внутрилабораторную воспроизводимость (коэффициент вариации CV, %) и правильность (уровень смещения среднего значения лаборатории от целевого значения) результатов исследований.
Низкий уровень обеспеченности клинико-диагностической лаборатории аттестованными контрольными материалами является ненадлежащим выполнением требований по контролю качества.
Документацией по ВЛК являются контрольные карты (с регистрацией результатов исследования контрольных проб и расчетом статистических показателей качества исследований в КДЛ) и журнал регистрации результатов исследований контрольных проб.
Для статистической отчетности в лаборатории необходимо вести дневники работы каждого специалиста (форма № 261-у), где ежедневно учитывается вся номенклатура выполненных им исследований. Ведется также дневник количества выполненных исследований по структурным подразделениям ЛПУ (обслуживаемых ЛПУ). На основании данных дневников ежемесячно заполняется «Журнал учета количества выполненных анализов в лаборатории» (форма № 262-у). При ведении журнала учета количества анализов допускается ведение отдельных страниц, посвященных:
– учету количества анализов по всей номенклатуре без разбивки по отделениям;
– учету количества анализов по отделениям без разбивки по всей номенклатуре, а лишь по группам исследований (биохимические, гематологические, общеклинические и др.).
Дополнительно ежемесячно рассчитывается нагрузка лаборатории (при необходимости – отделов лаборатории, отдельных сотрудников) в соответствии с нормативами затрат рабочего времени на лабораторные исследования и показатели уровня лабораторного обследования больных (количество анализа на больного, на койкодень, на 100 посещений).
14. Графики поверки средств измерений, свидетельства о поверке.
15.Копии заявок на приобретение контрольных и калибровочных материалов и сывороток, посуды, реактивов, технических средств и оборудования, стандартных образцов для градуировки и калибровки средств измерений. Степень удовлетворения заявок.
1.4. (1.6) Порядок работы иммунологической лаборатории. Материально-техническое оснащение, спектр лабораторных исследований иммунологической лаборатории
Основные задачи лаборатории - диагностика инфекций.
Прежде всего, это скрининг на инфицированность ВИЧ, гепатитами и сифилисом.
Лабораторная диагностика «ТОRCH - инфекций» у беременных женщин, или планирующих беременность:
определение антител к токсоплазмозу (IgM, IgG)
определение антител к цитомегаловирусу (IgM, IgG)
определение антител к вирусу простого герпеса 1,2 типов (IgM, IgG)
определение антител к хламидии (C. trachomatis) (Ig А, IgG)
определение антител к микобактерии туберкулеза (IgG)
Диагностика ревматоидных заболеваний, которая необходима больным с заболеваниями суставов и соединительной ткани:
определение антител к ДНК (определение аутоиммунной природы заболевания);
определение С реактивного белка, ревматоидного фактора, циркулирующих иммунных комплексов (ЦИК), иммуноглобулинов (IgА, IgM, IgG) - позволяет определить активность воспалительного процесса.
Исследование иммунного статуса.
Иммуногенетическое исследование, которое включает определение антигенов системы HLA, известное как «лейкоцитарные» или «тканевые» антигены.
Режим работы как в микробиологической лаборатории.
Помещения базовой лаборатории должны быть просторными для обеспечения безопасного проведения лабораторной работы. Стены, потолок, пол должны иметь гладкую, легко моющуюся поверхность, непроницаемую для жидкостей, устойчивую к дезинфектантам.
Лабораторию оснащают микроскопом, проточным цитометром, автоклавом, термостатами, сушильными, стерилизационными шкафами, аппаратом для свертывания сыворотки, дистиллятором, центрифугами, лабораторными весами, рН-метром, ФЭК, магнитной мешалкой, моечной ванной.
Рабочие помещения лаборатории должны быть снабжены подводкой холодной и горячей воды, электричеством, вакуумом, кис- лородом, воздухом высокого давления.
Располагают помещения таким образом, чтобы грязный и чистый потоки не перекрещивались и не соприкасались.
1.5. (1.7.) Порядок работы отдела ИФА. Материально-техническое оснащение, спектр лабораторных исследований отдела ИФА
Иммуноферментный анализ (ИФА) - это лабораторное исследование, основанное на реакции «антиген-антитело».
Суть метода - выявление специфических антител с помощью специальных биохимических реакций, которые помогают определить присутствие или отсутствие антител и их количество.
Методом ИФА можно определить уровень гормонов, иммуноглобулинов, иммунологических комплексов и других биологически активных веществ. Материалом для исследования может служить кровь (ИФА крови ), спинномозговая жидкость, содержимое стекловидного тела, околоплодные воды.
Метод иммуноферментного анализа используется для определения наличия антигенов возбудителей различных инфекций и для определения наличия антител классов (IgA, IgM, IgG) к антигенам различных возбудителей (вирусные гепатиты, ВИЧ, сифилис, TORCH, хламидиозы, паразитозы ).
Инфекции: гепатит А (антитела к ВГА), HBsAg, HBeAg, HBcAg, HBsAg подтверждающий, анти-HBsAg, анти-HBeAg, анти-HBcAg, гепатит C (антитела к ВГС), хламидиоз (антигены, IgG, A, M), трихомониаз (IgM), токсоплазмоз (IgG, M), лямблиоз, аденовирус (IgG, M), кандидозы, аспергиллез, болезнь Лайма, цитомегаловирус (IgG, M), вирус Эпштейна-Барра (IgG, M), ВИЧ 1,2 (антитела), вирус простого герпеса (IgG, M), вирус опоясывающего герпеса (IgG, M), вирус кори (IgG, M), вирус гриппа А,В (IgA, G, M), вирус парагриппа 1,2,3 (IgA, G, M), вирус паротита (IgA, G, M), вирус краснухи (IgG, M), кампилобактериоз (IgG, M), полиомиелит, дифтерия (IgG), эхинококкоз (IgG), сифилис (IgG, M), иерсиниоз, столбняк.
Опухолевые маркеры: альфа-фетопротеин, карциноэмбриональный антиген, простатспецифический антиген, CA-125, CA-15-3, CA-19-9, CA-242, ферритин, ХГЧ, NSE, тканевой полипептидный антиген, бета2-микроглобулин, UBC (рак мочевого пузыря).
Щитовидная железа: трийодтиронин (Т3), тироксин (Т4), тиреотропный гормон (ТТГ), тироглобулин, антитела к тироглобулину, антитела к тиреопероксидазе, антитела к микросомальным антигенам тиреоцитов.
Репродуктивная функция: пролактин, лютеинизирующий гормон (ЛГ), фолликулости-мулирующий гормон (ФСГ), хорионический гонадотропин человека (ХГЧ), антитела к сперме.
Эндокринология: кортизол, тестостерон, андростендион, прогестерон, адреналин, мелатонин, серотонин, СТГ, эстрадиол, эстриол, АКТГ, кальцитонин.
Аллергия: иммуноглобулин Е, антитела к аллергенам, гистамин.
Беременность: ХГЧ в моче и в сыворотке.
Аутоиммунные и системные заболевания: ревматоидный фактор, С-реактивный белок, АСЛО, антитела к ДНК и РНК (dsDNA, гистоны, SS-A, SS-B, RNP, Scl-70, Sm, Jo-I
высокая чувствительность, которая, составляющая 90%;
стабильность при хранении всех ингредиентов, необходимых для проведения ИФА (год и более);
быстрота и удобство проведения диагностической реакции;
возможность использовать минимальные объемы исследуемого материала;
возможность автоматизации всех этапов проведения реакции;
небольшая стоимость диагностических наборов;
возможность ранней диагностики инфекции;
унифицированность и пригодность для массовых обследований;
легкость в отслеживании динамики развития процесса инфекционного заболевания.
Метод позволяет различать острые и хронические формы заболеваний, выделять стадию заболеваний и выявлять практически здоровых носителей и контролировать вакцинацию.
Порядок работы, документация и оснащение – как в иммунологической лаборатории; вместо – проточного анализатора – иммуноферментный анализатор.
1.8. (1.9) Порядок работы ПЦР-лаборатории. Материально-техническое оснащение.
Спектр лабораторных исследований
Полимеразная цепная реакция (ПЦР) основана на амплификации (многократном увеличении числа копий) фрагмента ДНК-мишени в условиях in vitro и позволяет обнаружить специфичный участок генома микроорганизма.
в качестве экспрессного метода при исследовании материала от больного (подозрительного на заболевание) и индикации патогенных биологических агентов (ПБА) в объектах окружающей среды;
как ускоренный предварительный тест при выполнении культурального и биологического методов исследования и для идентификации подозрительных культур;
для определения эпидемиологической значимости изолятов на основании выявления генетических маркеров вирулентности, например, ctxA- и tcpA-генов у возбудителя холеры;
в научных целях для генотипирования штаммов или их ретроспективного анализа.
Требования к организации работ
Проведение исследований по выявлению ДНК (РНК) микроорганизмов I-II групп патогенности сопряжено с необходимостью одновременного обеспечения правил биологической безопасности работ и требований к организации и проведению ПЦР-анализа с целью предотвращения контаминации исследуемых проб нуклеиновыми кислотами (НК).
Противоэпидемический режим работы при ее организации и выполнении должен быть обеспечен в соответствии с СП 1.3.1285-03"Безопасность работы с микроорганизмами I-II групп патогенности (опасности)", регламентирующими работу с микроорганизмами I-II групп патогенности.
Все этапы исследования материала, зараженного или подозрительного на зараженность вирусами I группы, проводят в условиях максимально изолированных лабораторий с использованием изолирующих средств индивидуальной защиты или в боксах биологической безопасности III класса в защитном костюме IV типа, дополненном резиновыми перчатками.
Исследования материала, инфицированного микроорганизмами I-II групп патогенности, методом ПЦР проводят в организациях, имеющих лицензию на деятельность, связанную с возбудителями инфекционных заболеваний человека, в лабораториях, имеющих санитарно-эпидемиологическое заключение о возможности проведения соответствующих работ (с указанием конкретных видов микроорганизмов). В этой же лаборатории могут проводиться ПЦР-исследования с микроорганизмами III-IV групп патогенности.
Допускается проведение исследований крови методом ПЦР на бруцеллез, парентеральные вирусные гепатиты, ВИЧ-инфекцию в лабораториях, имеющих санитарно-эпидемиологическое заключение о возможности проведения работ с возбудителями III группы патогенности, выданное в установленном порядке.
Передачу исследуемого материала в другие организации проводят в соответствии с п.п.2.1.2 и 2.8.20 СП 1.3.1285-03"Безопасность работы с микроорганизмами I-II групп патогенности (опасности)".
Работу по ПЦР-диагностике организует специалист с высшим образованием, прошедший обучение на лицензированных курсах специализации (повышения квалификации) по работе с ПБА I-II групп патогенности и по ПЦР-диагностике.
Требования к помещению и оборудованию ПЦР-лабораторий
Помещения, в которых проводят исследования на наличие НК микроорганизмов I-II групп патогенности, размещают в "заразной" зоне лаборатории, проводящей диагностические и другие исследования с указанными микроорганизмами. При наличии возможности помещения располагают в виде отдельного блока. При строительстве новых или реконструкции имеющихся помещений лабораторию ПЦР размещают в отдельно стоящем здании (изолированной части здании) с соблюдением требований СП 1.3.1285-03"Безопасность работы с микроорганизмами I-II групп патогенности (опасности)" и учетом особенностей устройства вентиляционной системы ПЦР-лаборатории, изложенных в п.5.19 настоящих методических указаний.
Рабочая зона ПЦР-лаборатории в соответствии с этапами ПЦР-анализа должна включать следующий минимальный набор последовательно расположенных самостоятельных помещений или отдельно выделенных рабочих зон
(в составе других функциональных помещений):
приема, разборки, первичной обработки материала;
подготовки проб, выделения нуклеиновых кислот (НК);
приготовления реакционных смесей, проведения ПЦР и обратной транскрипции (ОТ);
учета результатов методом электрофореза или ГиФА.
Комнату выделения НК располагают вблизи от комнаты приема материала, а помещение для учета результатов - по возможности в отдалении от других перечисленных помещений для обеспечения условий, исключающих занос в них продуктов амплификации (ампликонов) с воздушным потоком.
Зону приема, регистрации, сортировки, первичной обработки материала (объединение или разделение проб, центрифугирование, инактивацию и т.д.) располагают в комнате приема материала блока для работы с инфицированными животными или в отдельной боксированной комнате. В этих же помещениях может проводиться обработка проб к другим видам исследований (бактериологическое, вирусологическое, серологическое и т.д.). При наличии возможности в помещении устанавливают бокс биологической безопасности III класса защиты.
Зону по подготовке проб и выделению нуклеиновых кислот размещают в боксированном помещении (микробиологический бокс с предбоксом).
Зону приготовления реакционных смесей и проведения ОТ и ПЦР-амплификации располагают в боксированном помещении или боксе биологической безопасности II класса (или ПЦР-боксе) - для подготовки реакционных смесей для ОТ и ПЦР.
При необходимости этап подготовки проб и выделения нуклеиновых кислот может выполняться в одной комнате с этапом ПЦР при наличии в ней бокса биологической безопасности II или III класса защиты для выделения НК и бокса биологической безопасности II класса (или ПЦР-бокса) - для подготовки реакционных смесей для ОТ и ПЦР. Каждый бокс рассматривается как соответствующая рабочая зона.
Зону детекции результатов располагают в боксированном помещении. При отсутствии боксированного помещения работу проводят в отдельной комнате, при возможности в ПЦР-боксе.
Помещения ПЦР-лаборатории покрывают кафелем (пол, стены) или масляной краской (стены, потолок), устойчивой к действию моющих и дезинфицирующих средств.
Во всех помещениях устанавливают бактерицидные лампы. Рекомендуется дополнительная установка переносного ультрафиолетового бактерицидного облучателя-рециркулятора.
Каждая рабочая зона должна иметь свой набор мебели, лабораторного оборудования, реагентов, автоматических пипеток, наконечников, пластиковой и стеклянной посуды, защитной одежды, обуви, резиновых перчаток, уборочного инвентаря и пр. используемых только в данной комнате (рабочей зоне).
В рабочих зонах должен быть свой набор холодильников.
Требования к проведению работ
Взятие материала производят согласно инструктивно-методическим документам, регламентирующим выполнение исследований для каждого вида возбудителя инфекций, инструкциям к тест-системам и в соответствии с СП 1.3.1285-03"Безопасность работы с микроорганизмами I-II групп патогенности (опасности)".
Транспортирование исследуемого материала и промежуточных продуктов ПЦР-анализа из одного помещения в другое при невозможности передачи их в смежные комнаты через шлюзовые передаточные окна, осуществляют в плотно закрывающихся контейнерах, обрабатываемых дезинфицирующими средствами после каждого переноса проб.
Доставку проб для исследования, а также их хранение осуществляют в закрывающихся металлических или пластмассовых контейнерах, на дне которых размещают адсорбирующий материал (марлевая салфетка, ткань, вата и пр.), смоченный раствором дезинфицирующего средства. Контейнер помещают в сумку-холодильник или в контейнер с хладагентами.
Манипуляции, сопровождающиеся риском образования аэрозоля (встряхивание, центрифугирование и т.д.) при обработке материала и выделении нуклеиновых кислот выполняют в боксах биологической безопасности II или III класса.
1.10. Методики выполнения анализов в биохимической лаборатории, ведение документации
Биохимическая лаборатория проводит биохимические, коагулологические, серологические исследования.
Показатели белкового обмена (альбумин, общий белок, электрофорез белков, креатинин, мочевина, мочевая кислота, тимоловая проба);
показатели липидного обмена (общий холестерин, холестерин ЛПВП, холестерин ЛПНП, триглицериды, индекс атерогенности);
показатели углеводного обмена (глюкоза, гликированный гемоглобин);
показатели пигментного обмена (билирубин общий, билирубин прямой);
показатели водно-солевого обмена (кальций, хлориды, железо, ОЖСС, калий, натрий, фосфор, магний, ферритин);
ферменты (АЛТ, АСТ, щелочная фосфатаза, амилаза, гамма-ГТП, КФК общая, ЛДГ общая, холинэстераза);
показатели гемостаза (протромбиновое время, фибриноген, АПТВ, этаноловый тест, РФМК, тромбиновое время, агрегация с АДФ, агрегация с ристомицином);
серологические исследования (группа крови, резус-фактор, антитела к резус-фактору, групповые антитела, СРП полуколичественно, АСЛО, АСК, ревмо-фактор, криоглобулины, антитела к ДНК); иммунноферментный анализ (ТТГ, Т4 свободный, альфа-ФП, СА-125, ПСА общий, ХГЧ).
Режим, оснащение, порядок работы – как иммунология и ИФА, оборудование – в обязательном порядке биохимический и иммунологический (при наличии заявленных услуг) анализаторы.

МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ
РОССИЙСКОЙ ФЕДЕРАЦИИ
от 21 декабря 1993 года N 295
Об утверждении положения об аккредитации
клинико-диагностических лабораторий
В целях подготовки лечебно-профилактических учреждений к работе в условиях бюджетно-страховой медицины и повышения эффективности их деятельности
Положение об аккредитации клинико-диагностических лабораторий (Приложение).
1. Министрам здравоохранения республик в составе Российской Федерации, руководителям главных управлений, управлений, департаментов и комитетов здравоохранения, Главного медицинского управления г. Москвы, руководителям лечебно-профилактических учреждений республиканского подчинения принять к руководству и исполнению утвержденное настоящим приказом Положение об аккредитации клинико-диагностических лабораторий.
2. Считать утратившим силу приказ Министерства здравоохранения СССР от 16 июля 1990 года N 285 "О введении в действие РД 42-19-301-90 "Методические указания по аттестации клинико-диагностических лабораторий".
3. Контроль за исполнением приказа возложить на первого заместителя Министра А.М.Москвичеева.
Приложение. Положение об аккредитации клинико-диагностических лабораторийПриложение к приказу
Министерства здравоохранения
Российской Федерации
от 21.12.93 N 295
1.1. Аккредитация клинико-диагностических лабораторий (КДЛ) проводится с целью установления и официального признания соответствия деятельности лаборатории установленным требованиям нормативно-технической документации (НТД). Лаборатория аккредитуется на заявленные виды деятельности.
1.2. Аккредитации подлежат как самостоятельные КДЛ, так и КДЛ в составе лечебно-профилактических учреждений (ЛПУ) независимо от подчиненности и форм собственности.
1.3. Аккредитация КДЛ и выдача сертификата осуществляются лицензионно-аккредитационными комиссиями, создаваемыми территориальными органами управления. Лицензионно-аккредитационные комиссии и территориальные органы управления здравоохранением создают комиссии по проверке КДЛ, в состав которых включаются представители органов здравоохранения, главные специалисты по лабораторной службе территории, высококвалифицированные специалисты в области лабораторной диагностики. По предложению лаборатории в состав комиссии могут быть включены дополнительно независимые эксперты с правом совещательного голоса. По результатам проверки КДЛ составляется акт (Приложение 4), на основании которого лицензионно-аккредитационная комиссия выдает сертификат (Приложение 5).
1.4. Работа по аккредитации КДЛ больниц и поликлиник республиканского подчинения и научно-исследовательских институтов, в том числе Российской Академии медицинских наук, усовершенствования врачей, института судебно-медицинской экспертизы проводится Российской лицензионно-аккредитационной комиссией, образованной Министерством здравоохранения России в соответствии с приказом Минздрава Российской Федерации от 28.06.93 N 148 .
1.5. Аккредитация КДЛ должна предшествовать или проводиться одновременно с аккредитацией ЛПУ, в состав которого входит КДЛ.
1.6. КДЛ может быть аккредитована независимо от результатов аккредитации ЛПУ, при этом КДЛ выдается сертификат.
1.7. Консультационно-методическую работу по аккредитации КДЛ осуществляют территориальные комиссии по лицензированию и аккредитации, Научно-методический центр по клинической лабораторной диагностике Минздрава Российской Федерации при ММА им.И.М.Сеченова. Организационное руководство осуществляет Управление медицинской помощи населению Минздрава Российской Федерации и территориальные органы управления здравоохранением.
1.8. Срок действия сертификата аккредитации не должен превышать 5 лет.
1.9. Органы управления здравоохранением организуют систематический инспекционный контроль за деятельностью аккредитованных КДЛ.
1.10. Оплата работы комиссий по аккредитации КДЛ производится за счет ЛПУ, в состав которого входит клинико-диагностическая лаборатория.
1.11. При несогласии КДЛ с решением комиссии по лицензированию и аккредитации она имеет право обжаловать это решение в третейской аккредитационной комиссии соответствующего территориального уровня.
2. Критерии аккредитации КДЛ на заявленные виды деятельности2.1. Наличие и соответствие условий деятельности КДЛ требованиям, установленным нормативно-технической документацией (НТД). К НТД относятся: приказы Минздрава Российской Федерации и территориальных органов управления здравоохранением, государственные и отраслевые стандарты, методические указания и инструкции по применению унифицированных клинических лабораторных методов исследования, утвержденные Минздравом СССР или Минздравом Российской Федерации, фармакопейные статьи; паспорта,технические описания и инструкции по эксплуатации приборов и применению наборов реактивов.
2.2. Наличие достаточного по количеству и квалификации персонала.
2.3. Соответствие помещений и условий работы КДЛ требованиям государственного санитарного надзора, государственного пожарного надзора, правилам техники безопасности.
2.4. Наличие оборудования, средств измерений, в том числе стандартных образцов, аттестационных смесей, вспомогательного оборудования, обеспечивающих надежное выполнение заявленных видов деятельности.
2.5. Наличие наборов реактивов, калибровочных и контрольных материалов, разрешенных Минздравом Российской Федерации к применению в здравоохранении, а также других химических реактивов, необходимых для проведения исследований в заявленной области.
2.6. Наличие на каждом рабочем месте инструкций, необходимых для проведения исследований и процедур.
2.7. Наличие в КДЛ инструкций по технике безопасности и производственной санитарии.
2.8. Проведение анализов и исследований в соответствии с унифицированными методами лабораторных исследований, утвержденными приказами Минздрава СССР и Минздрава Российской Федерации, инструкциями по применению наборов реактивов, разрешенным Минздравом Российской Федерации к использованию в КДЛ, или неунифицированными методами, утвержденными руководством ЛПУ.
2.9. Наличие в КДЛ регулярного внутрилабораторного контроля качества лабораторных исследований в соответствии с приказами Минздрава СССР от 16 апреля 1975 года N 380 "О состоянии и перспективах развития лабораторной клинико-диагностической службы в стране", от 23 апреля 1985 года N 545 "О дальнейшем совершенствовании контроля качества клинических лабораторных исследований".
2.10. Участие во внешнем (межлабораторном) контроле качества, осуществляемом на федеральном и региональном уровнях: наличие сертификата от органа, осуществляющего внешний контроль качества.
2.11. Наличие положения о КДЛ и должностных инструкций на каждого сотрудника КДЛ.
3. Порядок аккредитации КДЛ3.1. Аккредитация КДЛ предусматривает следующие этапы:
3.1.1. Подготовка КДЛ документов в соответствии с приложениями (Приложения 1-3) к настоящему положению.
3.1.2. Изучение и анализ документов, представленных КДЛ, лицензионно-аккредитационной комиссией и комиссией по проверке КДЛ.
3.1.3. Обследование КДЛ комиссией по проверке.
3.1.4. Оформление и выдача комиссией по проверке акта проверки КДЛ (Приложение 4).
3.1.5. Оформление, регистрация и выдача сертификатов лицензионно-аккредитационной комиссией (Приложение 5).
4. Права и обязанности аккредитационной КДЛ4.1. Аккредитованная лаборатория имеет право в пределах, определяемых сертификатом аккредитации:
- выполнять виды лабораторных исследований, указанные в сертификате;
- ссылаться на факт аккредитации КДЛ в выдаваемых документах и рекламных материалах;
- устанавливать собственные расценки на проведение аналитических исследований в аккредитованной области деятельности при оказании платных услуг;
- заключать с другими лабораториями и ЛПУ договоры на проведение конкретных анализов;
- при несогласии с решением лицензионно-аккредитационной комиссии опротестовать его в установленном порядке (Приказ Минздрава Российской Федерации от 20.03.92 N 93 "О мерах по выполнению закона Российской Федерации "О медицинском страховании граждан" ).
4.2. Аккредитованная КДЛ обязана:
- постоянно поддерживать свое соответствие критериям аккредитации;
- предоставлять возможность осуществлять инспекционный контроль за деятельностью лаборатории;
- подать заявку на аккредитацию за 3 месяца до истечения срока текущей аккредитации;
- не использовать права аккредитованной КДЛ по истечении срока действия сертификата аккредитации.
5. Лаборатория, претендующая на аккредитацию, подготавливает и представляет в лицензионно-аккредитационную комиссию следующие документы:5.1. Заявка (Приложение 1);
5.2. Копия ордера или договора об аренде помещения (для самостоятельных КДЛ);
5.3. Копия ранее выданных сертификатов и лицензий;
Примечание: для лабораторий, аттестованных в соответствии с приказом Минздрава СССР от 16.07.90 N 285 "О введении в действие РД 42-19-301-90 "Методические указания по аттестации клинико-диагностических лабораторий", дополнительно представляется акт и свидетельство об аттестации лаборатории.
5.4. Паспорт аккредитуемой лаборатории (Приложение 2) с указанием:
- информационных данных (Форма 1 паспорта);
- выполняемых видов лабораторных исследований на момент подачи заявки (Форма 2 паспорта);
- количества работающих в КДЛ сотрудников, их квалификационных характеристик (Форма 3 паспорта);
- сведения о помещении, оборудовании (Формы 4, 5, 6 паспорта);
- сведения о состоянии техники безопасности (Форма 6 паспорта);
- сведения о внутри- и межлабораторном контроле качества (Форма 7 паспорта и Приложение 3).
5.5. Копии сертификатов сотрудников, обеспечивающих выполнение заявленных видов деятельности.
5.6. Годовой отчет за последние 3 года работы КДЛ.
5.7. Заключение специалистов ПТО "Медтехника" о состоянии медицинского оборудования.
5.8. Заключение государственного санитарного надзора.
5.9. Заключение государственного пожарного надзора.
5.10. Заключение вышестоящих органов надзора по вопросам охраны труда и техники безопасности.
5.11. Заведующий КДЛ несет ответственность за правильность предоставляемой информации.
Начальник Управления
мед.помощи населению А.Д.Царегородцев
Приложение 1
к Положению об аккредитациии
клинико-диагностических
лабораторий
Председателю лицензионно-аккредитационной
комиссии
(Ф.И.О. адрес)
Наименование организации-заявителя
______________________________________________________________
Телефон Телефакс
______________________________________________________________
Прошу аккредитовать (наименование клинико-диагностической лаборатории) следующие виды исследований*.
* Перечень исследований может быть дан отдельным списком.
Заявитель обязуется принять комиссию, обеспечить условия для ее работы (проживание, транспорт, допуск в лабораторию, информацию, услуги по печатанию и размножению документов).
Заявитель гарантирует оплату расходов комиссии, связанных с процедурой аккредитации.
Главный врач лечебно-профилактического учреждения
______________________________________________________________
Заведующий клинико-диагностической лабораторией ______________
Главный бухгалтер ____________________________________________
Приложение 2. ПаспортПриложение 2
к Положению об аккредитациии
клинико-диагностических
лабораторий
Руководитель
(наименование лечебно-профилактического учреждения)
"___" ____________________ 19 г.
______________________________________________________________
(наименование клинико-диагностической лаборатории)
Заведующий клинико-диагностической лабораторией ______________
______________________________________________________________
(подпись)
Форма 1 к Паспорту
1. Наименование клинико-диагностической лаборатории
2. Юридический адрес
3. Ф.И.О. заведующего КДЛ и его телефон
4. Наименование лечебно-профилактического учреждения, в состав которого входит КДЛ
5. Ф.И.О. руководителя лечебно-профилактического учреждения, телефон
6. Ф.И.О. должностного лица, ответственного за контроль качества в КДЛ
Дата Заведующий клинико-диагностической
лабораторией _____________________
Форма N 2 к Паспорту
Дата Заведующий клинико-диагностической
лабораторией
Примечание: 1. В графе 3 указывают НТД: "униф.", если используется унифицированный метод, утвержденный приказом Минздрава СССР или РФ; "неуниф.", если используется унифицированный метод, утвержденный руководством ЛПУ; "инстр.", если используется инструкция к набору реактивов.
2. В графе 5 указывается: "лаб.", если готовятся отдельные реактивы в лаборатории, "набор", если используются готовые наборы, при этом указывается название набора, производитель, каталожный номер. В случае отсутствия наборов реактивов на момент аккредитации, указываются наборы, использованные в предшествующий период.
3. В графе 6 указывается "набор", если калибровочный раствор входит в состав набора реактивов: "калибр.", название, производитель и каталожный номер, если калибровочный раствор приготавливается в лаборатории.
Форма 3. Состав и квалификация персонала КДЛФорма 3 к Паспорту
1. Заведующий КДЛ
Об утверждении положения об аккредитации клинико-диагностических лабораторий