








/IMAGE/1289470372_60_1_1.gif)
 Рейтинг: 4.4/5.0 (1863 проголосовавших)
Рейтинг: 4.4/5.0 (1863 проголосовавших)Категория: Бланки/Образцы
Вопрос: Возможна ли продажа в аптеке отдельных таблеток в упаковке, не нарушая первичной упаковки, а просто допустим разрезая блистер на части? Как это оформить юридически и с точки зрения бухгалтерии? Какую информацию необходимо приложить к этой таблетке по закону (срок годности, инструкция)? Цель - сформировать конечный продукт - упаковку с несколькими отдельными препаратами, которые пациенту надо принять одновременно.
Вопрос относится к теме:
Вопрос: Медицинское оборудование планируется использовать при обучении, которое будет проводиться в виде проведения операций с использованием трупов людей. Возможна ли в дальнейшем реализация такого оборудования и использование его для операций над живыми пациентами?
Вопрос относится к теме:
Вопрос: На сайте Росздавнадзора есть файл в электронном виде, в котором систематизированы данные по зарегистрированным ценам ЖНВЛП. Также имеется файл, где содержится информация по исключенным позициям. В примечании написаны причины исключения. 1) исключения лекарственного препарата из перечня жизненно необходимых и важнейших лекарственных препаратов; 2) отмена решения о государственной регистрации или перерегистрации предельной отпускной цены производителя на лекарственный препарат; 3) представления производителем лекарственного препарата заявления об исключении сведений из реестра. В каких случаях лекарственное средство должно быть изъято из обращения?
Вопрос относится к теме:
Любое копирование и размещение информации на сторонних интернет-ресурсах возможно только при установке прямой индексируемой текстовой ссылки
на www.unico94.ru, в прочих сторонних источниках - только с письменного разрешения юридической компании "Юнико-94". Любые нарушения будут
рассматриваться и преследоватсья согласно статье 146 Уголовного Кодекса РФ "Нарушение авторских и смежных прав".
Продукты и услуги Информационно-правовое обеспечение ПРАЙМ Документы ленты ПРАЙМ Письмо Министерства здравоохранения РФ от 13 января 2014 г. № 25-4/10/2-79 О требованиях к обороту кодеинсодержащих препаратов и отпуску лекарственных препаратов, содержащих малые количества фенобарбитала
 Обзор документа
Обзор документа
Министерство здравоохранения Российской Федерации информирует о принятии Правительством Российской Федерации постановления от 16 декабря 2013 г. № 1159 «О внесении изменений в некоторые акты Правительства Российской Федерации по вопросам, связанным с оборотом наркотических средств и психотропных веществ» (далее - постановление).
Постановление вносит изменения в 5 постановлений Правительства Российской Федерации.
В частности, постановлением внесены изменения в раздел «Наркотические средства» списка II перечня наркотических средств, психотропных веществ и их прекурсоров, подлежащих контролю в Российской Федерации, утвержденного постановлением Правительства Российской Федерации от 30 июня 1998 г. № 681 (далее - перечень).
Изменения касаются приведения в соответствие двух норм, регламентирующих установление мер контроля в отношении препаратов, содержащих кодеин (его соли).
Первая норма определена пунктом 4 статьи 2 Федерального закона от 8 января 1998 г. № 3-ФЗ «О наркотических средствах и психотропных веществах» и регламентирует, что на препараты, содержащие наркотические средства (в том числе, кодеин), распространяются меры, аналогичные мерам контроля, предусмотренным к наркотическим средствам, содержащимся в них.
Другая норма, установленная перечнем, относила к наркотическим средствам 7 позиций лекарственных препаратов (в настоящее время не зарегистрированных и не представленных на фармацевтическом рынке России), содержащих кодеин от 10 мг до 30 мг на 1 таблетку/капсулу, в сочетании как с фармакологически активными ингредиентами, так и с нейтральными (фармакологическими неактивными) ингредиентами.
При этом ряд позиций лекарственных препаратов, содержащих кодеин до 20 мг, в соответствии с нормами приказа Минздравсоцразвития России от 16 марта 2010 г. № 157н «Об утверждении предельно допустимого количества наркотического средства, психотропного вещества и их прекурсора, содержащегося в препаратах» (далее - приказ Минздравсоцразвития России от 16 марта 2010 г. № 157н) отнесены к препаратам, содержащим малые количества наркотических средств.
Для указанных препаратов определены меры контроля только в части:
- отпуска физическим лицам по рецептам, а также запрета пересылки в почтовых отправлениях, в том числе международных (постановление Правительства Российской Федерации от 20 июля 2011 г. № 599 «О мерах контроля в отношении препаратов, которые содержат малые количества наркотических средств, психотропных веществ и их прекурсоров, включенных в перечень наркотических средств, психотропных веществ и их прекурсоров, подлежащих контролю в Российской Федерации») (далее - постановление Правительства Российской Федерации от 20 июля 2011 г. № 599);
- отпуска физическим лицам по рецептам, выписанным на рецептурных бланках формы № 148-1/у-88 (приказ Минздравсоцразвития России от 17 мая 2012 г. № 562н «Об утверждения Порядка отпуска физическим лицам лекарственных препаратов для медицинского применения, содержащих кроме малых количеств наркотических средств, психотропных веществ и их прекурсоров другие фармакологические активные вещества») (далее - приказ Минздравсоцразвития России от 17 мая 2012 г. № 562н).
Таким образом, требования к обороту кодеинсодержащих препаратов после принятия постановления не изменились:
1) для наркотических лекарственных препаратов, содержащих кодеин (в количестве более 20 мг на 1 дозу твердой лекарственной формы и более 200 мг на 100 мл/г жидкой лекарственной формы для внутреннего применения), остаются все меры контроля, предусмотренные законодательством о наркотических средствах и психотропных веществах в отношении кодеина (в том числе, отпуск по рецептам, выписанным на специальных рецептурных бланках формы № 107/у-НП, лицензирование всех видов оборота, установление особых требований к хранению и др.);
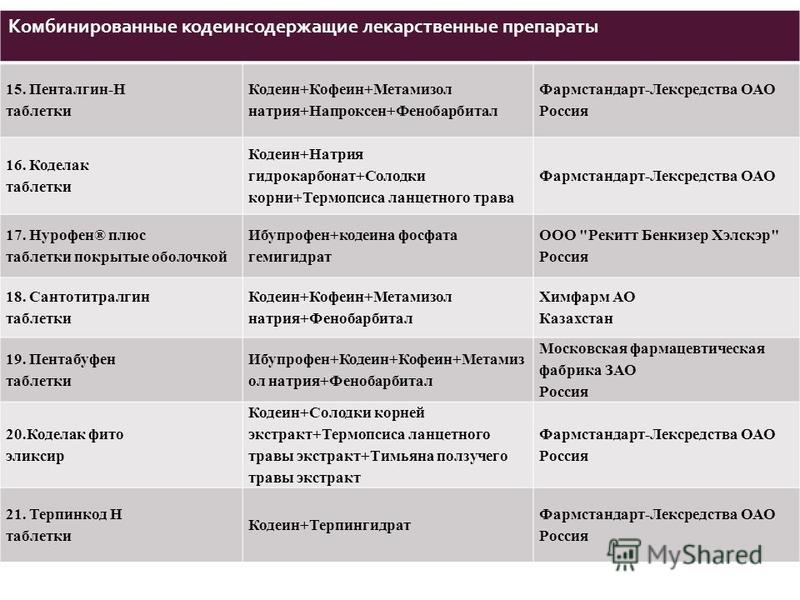
2) для лекарственных препаратов, содержащих малые количества кодеина (до 20 мг включительно на 1 дозу твердой лекарственной формы и до 200 мг включительно на 100 мл/г жидкой лекарственной формы для внутреннего применения), в частности «Седалгин», «Пенталгин», «Терпинкод», «Коделак фито» и др. остаются меры контроля, предусмотренные постановлением Правительства Российской Федерации от 20 июля 2011 г. № 599 и приказом Минздравсоцразвития России от 17 мая 2012 г. № 562н (в том числе, отпуск по рецептам, выписанным на рецептурных бланках формы № 148-1/у-88).
Кроме того, постановлением внесено изменение в Правила ведения и хранения специальных журналов регистрации операций, связанных с оборотом наркотических средств и психотропных веществ, утвержденные постановлением Правительства Российской Федерации от 4 ноября 2006 г. № 644, в части упрощения процедуры регистрации операций, связанных с оборотом наркотических средств и психотропных веществ, и предоставления права руководителю юридического лица устанавливать периодичность внесения записей в журнал регистрации операций, связанных с оборотом наркотических средств и психотропных веществ.
Введенная норма направлена на совершенствование обеспечения граждан лекарственными препаратами, в том числе содержащими наркотические средства и психотропные вещества, в связи со значительным расширением номенклатуры психотропных лекарственных препаратов, используемых в медицинских целях, после вступления в силу постановления Правительства Российской Федерации от 4 февраля 2013 г. № 78 «О внесении изменений в некоторые акты Правительства Российской Федерации».
Одновременно, в связи с поступающими обращениями, полагаем целесообразным обратить внимание на соблюдение требований по отпуску лекарственных препаратов, содержащих малые количества фенобарбитала.
В соответствии с нормами приказа Минздравсоцразвития России от 16 марта 2010 г. № 157н лекарственные препараты, содержащие фенобарбитал в количестве до 50 мг включительно на 1 дозу твердой лекарственной формы или до 2 г включительно на 100 мл/г жидкой лекарственной формы для внутреннего применения, в сочетании с иными фармакологическими активными компонентами, отнесены к лекарственным препаратам, содержащим малые количества психотропного вещества.
Таким образом, на указанные лекарственные препараты распространяются требования по отпуску, установленные приказом Минздравсоцразвития России от 17 мая 2012 г. № 562н:
1) лекарственные препараты, содержащие фенобарбитал в количестве, превышающем 20 мг и до 50 мг включительно на 1 дозу твердой лекарственной формы («Паглюферал 1», «Паглюферал 2», «Паглюферал 3»), отпускаются по рецептам, выписанным на рецептурных бланках формы № 107-1/у;
2) лекарственные препараты, содержащие фенобарбитал в количестве до 20 мг включительно в сочетании с эрготамином гидротартратом независимо от количества на 1 дозу твердой лекарственной формы («Беллатаминал»), отпускаются по рецептам, выписанным на рецептурных бланках формы № 107-1/у;
3) лекарственные препараты, содержащие фенобарбитал в количестве до 15 мг включительно в сочетании с кодеином (его солями) независимо от количества на 1 дозу твердой лекарственной формы («Пенталгин-Н», «Квинталгин», «Пиралгин», «Седал-М», «Седальгин-Нео», «Тетралгин» и др.), отпускаются по рецептам, выписанным на рецептурных бланках формы № 148-1/у-88;
4) лекарственные препараты, содержащие фенобарбитал в количестве до 20 мг включительно в сочетании с эфедрином гидрохлоридом независимо от количества на 1 дозу твердой лекарственной формы («Нео-Теофедрин», «Теофедрин-Н»), отпускаются по рецептам, выписанным на рецептурных бланках формы № 148-1/у-88;
5) лекарственные препараты, содержащие фенобарбитал в количестве до 20 мг включительно на 1 дозу твердой лекарственной формы («Андипал») или до 2 г включительно на 100 мл/г жидкой лекарственной формы для внутреннего применения («Валокордин», «Корвалол», «Валосердин»), отпускаются без рецепта.
Обзор документаВ декабре 2013 г. внесены изменения в ряд актов Правительства РФ по вопросам, связанным с оборотом наркотических средств и психотропных веществ (постановление от 16 декабря 2013 г. N 1159).
Разъяснено, что требования к обороту кодеинсодержащих препаратов не изменились.
Для наркотических лекарственных препаратов, содержащих кодеин (более 20 мг на 1 дозу твердой лекарственной формы и более 200 мг на 100 мл/г жидкой формы для внутреннего применения), остаются все меры контроля, предусмотренные в отношении кодеина (в т. ч. отпуск по рецептам, выписанным на специальных рецептурных бланках формы N 107/у-НП, лицензирование всех видов оборота, установление особых требований к хранению).
Для лекарственных препаратов с малым количеством кодеина (до 20 мг включительно на 1 дозу твердой формы и до 200 мг включительно на 100 мл/г жидкой формы для внутреннего применения) (в частности, "Седалгин", "Пенталгин", "Терпинкод", "Коделак фито") остаются следующее меры контроля. Предусмотренные постановлением Правительства РФ от 20 июля 2011 г. N 599 (в отношении препаратов, которые содержат малые количества наркотиков, психотропных веществ и их прекурсоров) и приказом Минздравсоцразвития России от 17 мая 2012 г. N 562н (в т. ч. отпуск по рецептам, выписанным на рецептурных бланках формы N 148-1/у-88).
Обращено внимание на требования по отпуску лекарственных препаратов, содержащих малые количества фенобарбитала.
По рецептам, выписанным на бланках формы N 107-1/у, отпускаются следующие препараты. Содержащие фенобарбитал в количестве от 20 мг до 50 мг включительно на 1 дозу твердой лекарственной формы ("Паглюферал 1", "Паглюферал 2", "Паглюферал 3"). Содержащие фенобарбитал в количестве до 20 мг включительно в сочетании с эрготамином гидротартратом независимо от количества на 1 дозу твердой лекарственной формы ("Беллатаминал").
По рецептам, выписанным на бланках формы N 148-1/у-88, отпускаются следующие препараты. Содержащие фенобарбитал в количестве до 15 мг включительно в сочетании с кодеином (его солями) независимо от количества на 1 дозу твердой лекарственной формы ("Пенталгин-Н", "Квинталгин", "Пиралгин", "Седал-М", "Седальгин-Нео", "Тетралгин"). Содержащие фенобарбитал в количестве до 20 мг включительно в сочетании с эфедрином гидрохлоридом независимо от количества на 1 дозу твердой лекарственной формы ("Нео-Теофедрин", "Теофедрин-Н").
Лекарственные препараты, содержащие фенобарбитал в количестве до 20 мг включительно на 1 дозу твердой лекарственной формы ("Андипал") или до 2 г включительно на 100 мл/г жидкой лекарственной формы для внутреннего применения ("Валокордин", "Корвалол", "Валосердин"), отпускаются без рецепта.
Для просмотра актуального текста документа и получения полной информации о вступлении в силу, изменениях и порядке применения документа, воспользуйтесь поиском в Интернет-версии системы ГАРАНТ:

Получите полный доступ к системе ГАРАНТ бесплатно на 3 дня!

© ООО "НПП "ГАРАНТ-СЕРВИС", 2016. Система ГАРАНТ выпускается с 1990 года. Компания "Гарант" и ее партнеры являются участниками Российской ассоциации правовой информации ГАРАНТ.
Все права на материалы сайта ГАРАНТ.РУ принадлежат ООО "НПП "ГАРАНТ-СЕРВИС". Полное или частичное воспроизведение материалов возможно только по письменному разрешению правообладателя. Правила использования портала.
Портал ГАРАНТ.РУ зарегистрирован в качестве сетевого издания Федеральной службой по надзору в сфере связи, информационных технологий и массовых коммуникаций (Роскомнадзором), Эл № ФС77-58365 от 18 июня 2014 года.
ООО "НПП "ГАРАНТ-СЕРВИС", 107076, г. Москва, ул. Стромынка, д. 19, к. 2, internet@garant.ru .
8-800-200-88-88
(бесплатный междугородный звонок)
Отдел рекламы: +7 (495) 647-62-38 (доб. 3153), adv@garant.ru. Реклама на портале.Медиакит
Если вы заметили опечатку в тексте,
выделите ее и нажмите Ctrl+Enter
 Согласно Постановлению Правительства РФ от 20.07.2011 г. № 599 (ред. от 22.12.2011 г.) «О мерах контроля в отношении препаратов, которые содержат малые количества наркотических средств, психотропных веществ и их прекурсоров, включенных в перечень наркотических средств, психотропных веществ и их прекурсоров, подлежащих контролю в Российской Федерации» установить норму по рецептурном отпуску комбинированных лекарственных препаратов, предназначенных для медицинского применения, содержащих малое количество кодеина или его солей, которая вводится в действие с 01 июня 2012 г.
Согласно Постановлению Правительства РФ от 20.07.2011 г. № 599 (ред. от 22.12.2011 г.) «О мерах контроля в отношении препаратов, которые содержат малые количества наркотических средств, психотропных веществ и их прекурсоров, включенных в перечень наркотических средств, психотропных веществ и их прекурсоров, подлежащих контролю в Российской Федерации» установить норму по рецептурном отпуску комбинированных лекарственных препаратов, предназначенных для медицинского применения, содержащих малое количество кодеина или его солей, которая вводится в действие с 01 июня 2012 г.
С 01 июня 2012 г. все комбинированные лекарственные препараты, содержащие кодеин или его соли в количестве до 20 мг на 1 дозу твердой лекарственной формы или до 200 мг на 100 мл/100 мг жидкой лекарственной формы для внутреннего применения, подлежат отпуску из аптек и аптечных пунктов по рецептам .
I. Для отпуска лекарственных препаратов
Применять форму рецептурного бланка: № 107-1/у «Рецептурный бланк» (срок действия рецепта 2 месяца или 1 год) и № 148-1/у-88 «Рецептурный бланк» (со сроком действия рецепта 10 дней или 1 месяц).
Норма отпуска лекарственных препаратов: по рецептурному бланку формы № 107-1/у «Рецептурный бланк» = не более 3-х лекарственных препаратов без каких-либо исправлений, а по рецептурному бланку формы № 148-1/у-88 «Рецептурный бланк» = только один лекарственный препарат без каких-либо исправлений.
Подлежат отпуску из аптек и аптечных пунктов по рецептам врача (фельдшера), выписанным на рецептурных бланках формы № 107-1/у, следующие комбинированные лекарственные препараты, содержащие:
а) кодеин или его соли в количестве до 20 мг (на 1 дозу твердой лекарственной формы), или до 200 мг (на 100 мл или 100 г жидкой лекарственной формы);
б) эрготамина гидротартрат в количестве до 5 мг (на 1 дозу твердой лекарственной формы);
в) декстрометорфана гидробромид в количестве, превышающем 10 мг, и до 30 мг (на 1 дозу твердой лекарственной формы).
Рецепты на комбинированные лекарственные препараты, выписанные на рецептурных бланках формы № 107-1/у (за исключением рецептов сроком действия до 1 года в соответствии с пунктом 1.17. Инструкции ), погашать штампом аптечной организации «Лекарство отпущено» и возвращаются больному на руки.
Для повторного отпуска указанных лекарственных препаратов сообщать больному об необходимости обратиться к врачу (фельдшеру) за новым рецептом.
При отпуске комбинированных лекарственных препаратов по рецептам врача (фельдшера), выписанных на рецептурных бланках формы № 107-1/у, и действующим в течение 1 года, рецепт возвращается больному с указанием на обороте наименования или номера аптечной организации, подписи работника аптечной организации, количества отпущенного препарата и даты отпуска.
При очередном обращении больного в аптечную организацию учитываются отметки о предыдущем получении лекарственного препарата. По истечении срока действия рецепт гасится штампом «Рецепт недействителен» и оставляется в аптечной организации.
ВНИМАНИЕ: В связи с вышедшими разъяснениями от Министерства Здравоохранения, отпуск кодеинсодержащих препаратов производится только по 148-1/у-88 рецептурному бланку.
II. Oтпуск ниже перечисленных препаратов производить строго по рецепту, оформленному по всем требованиям приказов МЗ, включая СРОК ДЕЙСТВИЯ РЕЦЕПТА.
Обеспечить хранение данных препаратов по списку Б:
Гликодин сироп 100 мл
Гриппекс №10, №20, №100 табл.
Грипэнд №12, №24 табл. №6, №60 пак.
Каффетин №10, №12 табл.
Каффетин-колд №10 табл.
Коделак №10 табл.
Коделак сироп 100 мл
Кодтерпин № 10 табл.
Но-шпалгин тбл №12
Нурофен плюс №12 табл.
Пенталгин ICN №12 таб.
Пенталгин Н №10 табл.
Пенталгин плюс №12 табл.
Пиралгин №10 табл.
Седал-М №10, №20 табл.
Седальгин-Нео №10 табл.
Солпадеин №12 капс.
Солпадеин №12 табл. пластиковая упаковка
Солпадеин №12 табл. растворимые
Солпадеин №8 табл.
Терпинкод №10 табл.
Тетралгин №10 табл.
Тофф плюс №10 капс.
Туссин Плюс сироп 118 мл
Юниспаз №12 табл.
© 2004 ООО "ИФК Аптеки". Все права защищены.
Использование материалов и графики с сайта без согласования с администрацией запрещено.
Внимание! Информация, размещенная на сайте, не является основанием для самолечения.
Перед применением препарата необходимо проконсультироваться с врачом.
Аптека-онлайн, служба доставки лекарств, дежурная аптека онлайн
Экзаменационный билет №19
1. Фармацевтическая фирма-дистрибьютер закупила таблетки фенобарбитала и бензонала. В целях исключения возможной фальсификации Вам необходимо установить подлинность действующих веществ в таблетках и оценить их качество.
Приведите химические формулы фенобарбитала и бензонала, охарактеризуйте химическое строение каждого из них.
Обоснуйте возможность использования физико-химических свойств для оценки качества, приведите нормативные показатели. Предложите групповые и дифференцирующие реагенты для установления подлинности каждого из них, обоснуйте условия проведения реакций.
Обоснуйте возможные методы количественного определения в субстанции и таблетках, приведите расчетные формулы.
Фенобарбитал (Phenobarbitalum,Phenobarbital)

Функц Гр: основа – лактамная форма барбитуровой к—ты, 2 имидных группы
Бел крист порошок без запаха, горького вкуса, р-рим в эфире, 95% спирте, р-рах щелочей, очень мало в холодной воде, трудно в горячей воде, хлороформе.

Функц Гр: Функц Гр: основа – лактамная форма барбитуровой к—ты, имидная и амидная группы Белый крист порошок, очень мало р-рим в воде, легко в хлороформе, р-рим в эфире, трудно р-рим в спирте
2. Фенобарбитал: ПОДЛИННОСТЬ: 1.ИК 2.Tпл=174-178 3. Хим р-ции. 1. Общей гр реакцией на все барбитураты является р-я комплексообразования с солями кобальта (кроме тиопентала-натрия). 0,05 препарата р-ряют в 2 мл 95% спирта, прибавляют 1 каплю кальция хлорида, 2 капли р-ра нитрата кобальта, 2 каплиNaOH, появляется сине-фиолетовое окрашивание. Реакция основана на образовании комплексных соли.
2. Реакция комплексообразования с меди сульфатом в присутствии карбоната и гидрокарюоната калия. Барбитураты образубт комплексные соединения, имеющие различную окраску: 0,1 препарата взбалтывают с 1мл 1% NaOH, прибавляют 0,2 мл р-ра карбоната и гидрокарбоната калия, 0,1 мл сульфата меди, образуется осадок бледно-сиреневого цвета, не изменяющийся при стоянии, засчет образования комплексной соли.

Примеси: хлориды, сульфаты, фенилбарбитуровая к-та (с метиловым красным), орг примеси, сульфатная зола, тяжелые металлы. (см по ГФ)
Препараты лактамной (кислотной) формы количественно определяют методом КО-титрования. В качестве протофильного растворителя исполбзуют ДМФА. Титрант – 0,1 М р-р натрия гидроксида в смеси метанола и бензола. Индикатор – тимоловый синий.
В ТЭ р-р приобретает синее окрашивание.
При количественном определении фенобарбитала лекарственное вещество растворяют в ацетоне или спирте, прибавляют необходимое количественное воды и титруют 0,1М раствором натрия гидроксида в присутствии индикатора тимолфталеина. Применение данной методики показывает, что фенобарбитал обладает достаточно выраженными кислотными свойствами и может достоверно количественно определяться и в водной среде. Ацетон (или спирт) препятствуют гидролизу образующейся при титровании соли.
Бензонал: ПОДЛИННОСТЬ: 1. ИК. 2. Тпл=134-138, 3. Хим р-ции 1) аналогична 1ой р-ции фенобарбитала. 2) к 0,2 преп + 10 кап 1% р-раNaOH, 0,2 мл р-ра карбоната и гидрокарбоната калия, 0,1 мл сульфата меди, появлсеро-голубое окрашивание.
Остальное аналогично фенобарбиталу.
Конденсация с ароматическими альдегидами
Барбитураты способны к конденсации с альдегидами в присутствии концентрированной
серной кислоты как водоотнимающего и окислительного реагента. При выборе соответствующего альдегида и условий можно получить специфически окрашенный продукты, позволяющие идентифицировать отдельный лекарственные вещества.


Фенобарбитал имеет в 5-м положении фенильный радикал, по которому возможны Se-реакции, например нитрование с последующим восстановлением нитрогруппы, диазотированием и азосочетанием
Фрагмент бензойной кислоты в бензонале открывают после гидролиза взаимодействием с солями трехвалентного железа (появляется осадок оранжево-желтого цвета). По амидной группе препарат вступает в реакцию гидроксамовой пробы.
Гидроксаматы железа представляют собой растворы красно-фиолетового цвета, а гидроксаматы меди – осадок бирюзового цвета.
Количественное определение индивидуальных препаратов, особенно для их ЛФ применяют физико-химические методы анализа, такие как ВЭЖХ, ТСХ, ГЖХ, спектрофотомерия. Также можно использовать гравиметрию и аргентометрию в прямом и обратном вариантах.

2. В аптеку поступил рецепт на изготовление порошков.
•Проведите фармацевтическую экспертизу прописи рецепта. При необходимости внесите изменения в пропись в соответствии с НД.
Papaverini hydrochloridi 0,04
Misce fiat pulvis
Signa:no1 порошку 2 раза в день.
Примечание. Учитывая, что все вещества измельчаются в одной ступке, коэффициент рабочей поверхности можно не учитывать.
Выберите вещество для операции предварительного измельчения с целью уменьшения потери веществ в ступке*. Выбор обоснуйте, выполнив соответствующие расчеты.
Проведите оценку качества препарата на стадиях изготовления, изготовленной лекарственной формы и контроля при отпуске.
•- значение абсолютной потери (мг) при диспергировании в ступке № 1: кодеин - 7; фенобарбитал - 18; папаверина гидрохлорид - 10; фенацетин - 19; анальгин - 22.
Выписан рецепт на твёрдую лекарственную форму для вагинального применения. Форма бланка: 148 - 1 /у - 88, рецепт хранится в аптеке 5 лет. Больному выписывается сигнатура.
Кодеин, фенобарбитал - вещества, находящиеся на предметно - количественном учёте и для изготовления лекарственных форм отпускаются только провизором - технологом и составляется акт приёмки - передачи, кроме того кодеин имеет норму единовременного отпуска - 0,2. В рецепте выписано: 0,015*10=0,15 кодеина, что не превышает н.е.о.
Заключение: дозировка лекарственных веществ не завышена, лекарственную форму можно готовить. Изготавливают лекарственную форму с соблюдением санитарных требований (Пр.МЗРФ№309)
Первым в ступку помещают фенацетин как вещество общего списка и имеющего наименьшие относительные потери.
Расчет: кодеин и фенобарбитал в ступку первыми не помещают, т.к. эти вещества находятся на ПКУ
Папаверина г/хл имеет потери 10 мг, его общее количество, выписанное в рецепте: 0,04*10=0,4, потери в % - 1:0,4=2,5%. Фенацетина - 1,9/2,5=0,76%. Анальгина - 2,2/2,5=0,88%.
Таким образом в ступку первым помещают фенацетин.
Соотношение веществ в составе порошков: 1:16:2,5:6 не превышает соотношение 1:20 -порошки можно готовить, не отсыпая на капсулу, помещая все вещества сразу от меньшей массы к большей. Кодеин добавляют вторым, предварительно смешав приблизительно с равным количеством порошка, затем добавляют остальную часть и тщательно смешивают.
Отпускаются порошки в вощаных капсулах в бумажном пакете, т.к. анальгин - гигроскопичное вещество.
Этикетка с указанием: «Внутренне» (зелёный сигнальный цвет), дополнительно - «Хранить в сухом, прохладном, защищенном от света месте». Срок годности: 10 суток.
Общая масса 6,55
Папаверина г/хл 0,4
Общая масса 6,55 м
1 порошка = 0,65 н.д.о. +/- 5% (+/-0,03) 0,62..0,68
Подготовить рабочее место, подобрать вспомогательный материал.
На BP г/п 5,0 отвесить 2,5 фенацетина - поместить в ступку, растереть, затерев поры. У провизора - технолога получить 0,15 кодеина - поместить в ступку, смешать. На BP г/п 1,0 отвесить 0,4 папаверина г/хл - поместить в ступку, смешать. У провизора - технолога получить 1,0 фенобарбитала - поместить в ступку, смешать. На BP г/п 5,0 отвесить 2,5 анальгина -поместить в ступку, смешать до однородности, проверить на однородность.
На BP г/п 1,0 развесить 10 порошков по 0,65, завернуть их в вощаные капсулы, поместить в бумажный пакет, снабдить этикетками. По памяти заполнить ППК, на обратной стороне которого делают пометку о получении кодеина и фенобарбитала (наименование, отпущенная масса вещества - цифрами и прописью, отпустил, получил и дата).
3. Приведите нормативное обоснование требованиям к оформлению рецепта на экстемпоральное изготовление порошков по данной прописи, выписанного бесплатно. Укажите сроки действия и хранения рецепта в аптеке.
Количество каких ингредиентов, входящих в пропись, нормируется при отпуске из аптек по экстемпоральным рецептам? Ответ обоснуйте.
Имеются ли среди ингредиентов данной прописи подлежащие предметно-количественному учету в аптеке? Если имеются, назовите их. Каков порядок предметно-количественного учета этих ЛП в аптеке?
Фенобарбитал – сильнодействующее вещество, перечень таких веществ утверждается Постановлением Правительства РФ от 25.12.2007 № 964 ( с изм.).
Кодеин - наркотическое вещество списка ?? ФЗ. Перечень этих веществ утвержден Постановлением Правительства РФ № 681 от 30.06.1998 г. (с изм.) «Перечень наркотических средств, психотропных веществ и их прекурсоров, подлежащих контролю в РФ».
Согласно приказа МЗ и СР РФ № 110 от 12 02 07 «О порядке назначения и выписывания лекарственных препаратов, изделий медицинского назначения и специализированных продуктов лечебного питания» и приказа МЗ и СР РФ № 785 от 14.12.2005 «О порядке отпуска ЛС» рецепт на данную лек. форму выписывается на рецептурном бланке формы № 148-1/У-88, так как рецепт выписан для бесплатного отпуска, то кроме этого бланка нужен бланк формы № 148-1/У-04 (Л) или № 148-1/У-06 (Л). Последние 2 бланка выписываются в трёх экземплярах, один из которых сразу подклеивается в амбулаторную карту больного, а 2 экземпляра предъявляются в аптеку.
Рецепты оформляются штампом МО, подписью и личной печатью врача, печатью МО «Для рецептов», срок действия рецептов 10 дней. Рецепты остаются в аптеке, и хранятся для бесплатного отпуска 5 лет, а так как в бланке формы № 148-1/У-88 выписано наркотическое вещество Кодеин, то эти бланки хранятся 10 лет.
При отпуске необходимо проверить норму отпуска кодеина, она не должна превышать 0,2.
В данном случае она не превышена. Норма отпуска барбитуратов в приказе № 110 указана в таблетках и не должна превышать 10-12 таблеток.
Приказом МЗ и СР РФ от 14.12.05 № 785 утверждён перечень ЛС, подлежащих ПКУ в аптечных учреждениях, организациях оптовой торговли ЛС, мед оррганизациях».
Постановлением Правительства РФ № 644 от 04.11. 06 « О порядке предоставления сведений о деятельности, связной с оборотом наркотических средств, ПВ» учет ведется в «Журнал регистрации операций, связанных с оборотом наркотических средств и психотропных веществ», пронумерованном, сброшюрованном, заверенном подписью руководителя аптеки, скрепленном печатью организации. Форма Журнала утверждается руководителем аптеки. На Кодеин (субстанция) заводится отдельный журнал. Лицо, на которое приказом руководителя возложена ответственность за ведение и хранение журнала, записи производит в хронологическом порядке непосредственно после каждой операции, связанной с оборотом НС и ПВ, на основании документов, подтверждающих совершение этой операции. Эти документы подшивают в отдельную папку, которая хранится вместе с Журналом регистрации. Нумерация записей осуществляется в пределах календарного года в порядке возрастания номеров. Каждая запись в Журнале заверяется подписью М.О. лица с указанием ФИО. Подчистки и незаверенные М.О. лицом исправления не допускаются. Не реже 1 раза в месяц МОЛ проверяет записи в Журнале и ставит свою подпись. Журнал регистрации хранят в сейфе, ключи от которого находятся у ответственного за ведение и хранение Журнала. Заполненный Журнал хранится в организации 10 лет после внесения последней записи. Затем он подлежит уничтожению, при этом составляется акт, подтверждаемый руководителем организации.
Юридические лица, имеющие лицензии на осуществление видов деятельности, связанных с оборотом НС и ПВ, ежеквартально и ежегодно представляют отчёты о своей деятельности, количестве каждого изготовленного, везённого, реализованного, использованного ЛС этой группы, а также сведения о запасах по состоянию на 31 декабря отчётного года. Постановление Правительства РФ №644 от 04.11.06г. «О порядке предоставления сведений, о деятельности связанной с оборотом наркотических средств, психотропных веществ».
Фенобарбитал также подлежит ПКУ и учитывается в «Журнале учета ядовитых, других медикаментов и этилового спирта». страницы которого также пронумерованы, прошнурованы и заверены подписью руководителя аптеки, скреплены печатью организации. На каждое наименование в этом Журнале заводится отдельная страница. Остаток на начало месяца переносится из остатка на конец предыдущего месяца. Данные в приход – на основании товарно – сопроводительных документов при поступлении со склада. Данные в расход записываются ежедневно по мере расхода на основании Дневного выборочного листа, где ведётся отдельный учёт расхода: по рецептам и по требованиям МО. В конце месяца подсчитывают общий расход и выводят остаток на конец месяца по формуле: Ок = Он + П – Р. Фактический остаток определяется путем взвешивания и сравнивается с книжным остатком. Если обнаружена недостача, то есть Ок > Оф, то к количеству израсходованным по рецептам индивидуального приготовления ЛС применяются нормы естественной убыли, которые составляют:
0,95% от израсходованного количества по амбулаторной рецептуре
0,4% от количества, отпущенного в виде АНГРО (в МО).
До проведения инвентаризации несмотря на расхождения, на начало следующего месяца переносится книжный остаток и только после инвентаризации – фактический.
4. Дайте характеристику природному растительному источнику кодеина и папаверина:
Приведите пример с латинскими названиями растения, сырья, семейства. Укажите сырьевую базу.
Какие методики существуют в фармакогностическом анализе для подтверждения присутствия и содержания алкалоидов в лекарственном растительном сырье? Приведите примерную схему методики количественного определения с объяснением выбора экстрагента, условий экстракции, очистки и собственно количественного определения.
Каковы условия хранения лекарственного сырья, содержащего папаверин?
Алкалоиды папаверин и кодеин получают из коробочек мака снотворного.
Коробочки мака — Сарitа Рараveris
Мак снотворный (мак опийный) Рараvегsomniferum
Семейство маковые — Рараveraceae
В диком виде не встречается. Родина мака Средняя Азия. Опийные и масличные сорта мака культивируются в Иране, Афганистане, Турции, Китае и др. Мак импортируется из Азии.
Для обнаружения алкалоидов применяют реакции, в результате которых образуются осадки или характерное окрашивание. Папаверин и кодеин относятся к производным изохинолина.

1.Для подтверждения содержания алкалоидов в сырье проводят общие реакции.
Общие реакции осаждения. Позволяют установить присутствие алкалоидов даже при незначительном их содержании. Из общих алкалоидных реактивов часто используют следующие: танин, дихлорид ртути, раствор йода в иодиде калия, пикриновую и фосфорномолибденовую кислоты и др. которые дают осадки разного цвета.
2. Специальные цветные реакции. Применяют при анализе отдельных алкалоидов - чистых или с очищенными извлечениями. Наиболее распространенные реактивы - концентрированная серная и азотная кислоты, раствор формалина в серной кислоте.
3.Специальная реакция на кодеин.
С реактивом Марки кодеин дает синее окрашивание.
Реактив Марки? — реактив, применяемый в аналитической и токсикологической химии для качественного обнаружения алкалоидов и других азотистых оснований .Реактив Марки представляет собой концентрированную серную кислоту с добавлением формалина в соотношении 1 капля формалина на 1 миллилитр серной кислоты. Для корректного обнаружения реактив должен быть свежеприготовленным. Реактив Марки применяется в качестве проявителя при обнаружении алкалоидов. лекарственных средств и наркотических веществ в крови. моче и трупном материале методом тонкослойной хроматографии .
Основной цветной реакцией на папаверин гидрохлорид является его взаимодействие с концентрированной азотной кислотой, при котором появляется желтое окрашивание, а при нагревании на водяной бане окраска становится желто-оранжевой.
Количественное определение проводят по индивидуальным методикам.
Этапы количественного определения:
1. Извлечение суммы алкалоидов из сырья.
Алкалоиды извлекают в виде солей или в виде оснований.
В первом случае сырье обрабатывают слабыми растворами органических или минеральных кислот, соли которых хорошо растворимы в воде или спирте. Используют винную, лимонную, уксусную, серную, соляную и другие кислоты.
Во втором случае сырье смачивают концентрированным раствором аммиака. Едкие щелочи не используют, т. к. они образуют феноляты, вызывают гидролиз, изомеризацию алкалоидов. Раствор аммиака вытесняет алкалоиды-основания из солей. Алкалоиды-основания извлекают органическими растворителем (эфир, хлороформ, бензол и др).
Извлечение проводят многократно новыми порциями до полного истощения сырья. Полученные порции объединяют.
2. Очистка извлечения от балластных веществ. Проводят путем двух или трехкратной сменой растворителя.
3. Разделение суммы алкалоидов и выделение индивидуальных алкалоидов.
Методы количественного определения кодеина и папаверина.
Кодеин выделяют х/ф из ЛРС в виде основания. Титруют раствором соляной кислоты до розового окрашивания. Индикатор - метиловый красный.
Папаверин выделяют в виде хлористоводородной соли. Титруют раствором щелочи до розового окрашивания. Индикатор фенолфталеин.
Лекарственное растительное сырье, содержащее папаверин и кодеин, хранят с предосторожностью, в сухом хорошо проветриваемом помещении, отдельно от других видов сырья по списку А.
Кодеин применяется в виде оснований и фосфата в таблетках. Оп уменьшает возбудимость кашлевого центра, его назначают при кашле.
Папаверина гидрохлорид - это миотропный спазмолитик (снимающий спазмы гладкой мускулатуры) понижает тонус и уменьшает сократительную деятельность гладких мышц и оказывает в связи с этим сосудорасширяющее и спазмолитическое действие. В больших дозах понижает возбудимость сердечной мышцы, замедляет внутрисердечную проводимость.
Применяют при спазмах сосудов головного мозга, стенокардии, эндартериите, холецистите, спастическом колите, почечной колике, бронхоспазмах. Выпускают в виде порошка, таблеток и ректальных суппозиториев.
Морфин, применяют как болеутоляющее средство при болях, при подготовке к операции и в послеоперационном периоде, понижает возбудимость дыхательного и кашлевого центров, оказывает снотворное действие, тормозит двигательную функцию желудка и кишечника. Повторные приемы морфина ведут к привыканию и пристрастию к нему, сопровождающемуся тяжелыми психическими расстройствами и поражением всех органов.
Кодеин, снижает возбудимость кашлевого центра, применяется главным образом от кашля.
Папаверин широко применяется как спазмолитическое средство при гипертонии, стенокардии, мигрени, пилораспазме, холецистите, спастическом колите, спазме мочевых путей, бронхиальной астме; оказывает успокаивающее действие на центральную нервную систему, снижает тонус гладкой мускулатуры и расслабляет ее.
5. На фармацевтическом производстве выпуск представленных лекарственных препаратов (таблеток фенобарбитала и бензонала) осуществляется в соответствии с ПР.
Охарактеризуйте основные группы вспомогательных веществ, применяемые в таблеточном производстве.
Объясните сущность процесса гранулирования. Что такое сухое гранулирование? Предложите оборудование для данного вида гранулирования.
Производство галеновых препаратов и готовых лекарств осуществляется по заранее разработанным и утверждённым регламентам, т.е. по правилам, устанавливающим определённый порядок работы. Регламент разрабатывается экспериментальными лабораториями предприятий или по заданиям предприятий НИИ или кафедрами вузов. Сначала идёт процесс изучения технологии внедряемого препарата или готового лекарства на небольших порциях и малогабаритной (полузаводской) установке, а затем на опытной партии и цеховой аппаратуре.
Регламенты для фармацевтических предприятий утверждается соответствующим учреждением Мин.Здрава. Регламенты разрабатываются исходя из фактической оснащенности предприятия и технических норм, которым должна отвечать готовая продукция по ГФ или ГОСТам.
Регламенты включают следующие разделы:
Характеристика готовой продукции (по ГФ или ГОСТу). Указывается характер упаковки, условия хранения и назначение препарата.
Характеристика исходного сырья. В табличной форме приводятся основные показатели исходных сырьевых материалов со сносками на ГФ и ГОСТ.
Технологическая схема производства - приводится в виде материального потока с указанием всех операций и связанных с ними исходных материалов, побочных продуктов, отбросов и готового продукта.
Спецификация аппаратуры и оборудования. В табличной форме приводится перечень аппаратов и оборудования с указанием их количеств, материалов, из которых они изготовлены, и характеристика аппаратов с указанием их ёмкости, формы, габаритов и других признаков. В этот же раздел включается и аппаратурная схема производства, состоящая из схематического чертежа производственного потока с условным изображением аппаратов, цифровые обозначения которых приводятся под чертежом.
Описание технологического процесса. Оно должно быть подробным, последовательным, с ссылками на аппаратную схему производства.
Нормы времени на проведение технологических операций. В этом разделе регламентируется продолжительность отдельных операций (в минутах и часах). В конце выводится продолжительность всего производственного процесса и подсчитывается годовая мощность производства по ведущим операциям.
7. Отходы производства.
Техника безопасности (особо отмечается: наиболее опасные моменты, приводятся соответствующие инструкции).
Методы анализа и контроль производства (указания: кто, где, когда и как проводит анализы со ссылкой на ГФ, ГОСТ, ТУ или ВТУ и др.).
Расходные нормы. Приводятся расчеты на 1000 кг или 100 кг готового продукта для сырья, вспомогательных материалов и энергетики, также параллельно указывается расход по расчетным данным (фармацевтической прописи).
Основные группы вспомогательных веществ для таблетирования.
Все вспомогательные вещества придают порошку определённые свойства, влияя не только на качество ЛФ, но и на её доступность, поэтому подбор вида и количества вспомогательных веществ должно быть научно - обоснованным.
Все вспомогательные вещества по назначению делятся на несколько групп:
Наполнители (разбавители) - вещества, использующиеся для придания таблетке определённой формы при небольшой дозировке действующего вещества (сахароза, глюкоза, лактоза); с целью повышения растворимости трудно растворимых гидрофобных веществ применяются водорастворимые наполнители (разбавители).
Связывающие (склеивающие) вещества - применяются для гранулирования и обеспечения необходимой прочности гранул и таблеток. Для этих целей используются: вода, спирт, раствор крахмала, желатозы и др.
Разрыхлители - применяются для обеспечения необходимой распадаемости таблеток и рас творения лекарственных веществ. По механизму действия разрыхлители делятся на три группы:
• Набухающие вещества - разрывают таблетку при набухании в жидких средах - порошок альгиновой кислоты, амилопектин и др.
• Вещества, улучшающие смачиваемость и водопроницаемость - крахмал, твин - 80.
• Газообразные вещества - смесь водных винной/лимонной кислоты с натрия гидрокарбонатом или кальция карбонатом - при растворении компоненты смеси выделяют углекислый газ и разрывают таблетку.
4. Скользящие (смазывающие) вещества - антифрикционные, антиадгезионные - уменьшают
трение частиц друг с другом и поверхностью прессующего инструмента. Вещества используются
в качестве наимельчайших порошков. Они подразделяются на две группы:
Скользящие - улучшающие сыпучесть таблеточных смесей (крахмал, тальк, аэросил, ПЭО -400).
Смазывающие вещества - снижающие силу выталкивания таблетки из матрицы (кислота стеариновая и её соли, тальк, воск, ПЭО - 400)/
Кроме того все скользящие вещества предотвращают налипание порошка на пуансоны и стенки матриц и снимают электростатические заряды с поверхности частиц.
Красители - добавляются в состав таблеток для улучшения внешнего вида и обозначения терапевтической группы.
Корригенты - вещества, улучшающие органолептические свойства таблетки, улучшая её вкус и запах (сахар, ваниль, какао).
Ввиду проявления нежелательных эффектов количество некоторых вспомогательных веществ в составе таблеток ограничивается.
Например, по ГФ XI твина - 80, стеариновой кислоты - не более 1%, талька - 3%, аэросила -10% от массы таблетки.
Гранулирование - это процесс превращения порошкообразного материала в частицы определённой величины различают:
• Влажное гранулирование - с увлажнением до или в процессе грануляции.